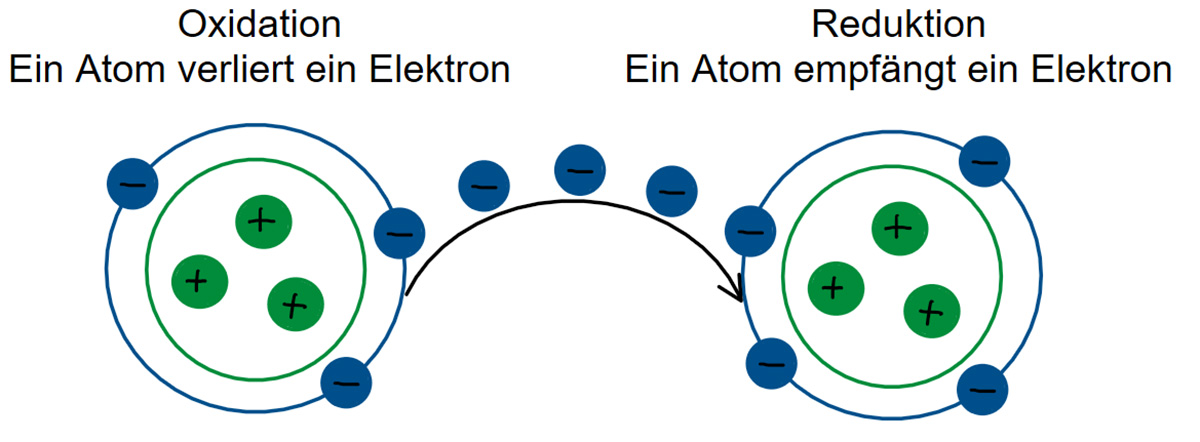
Was ist eine Redoxreaktion?
Eine Redoxreaktion ist eine chemische Reaktion, bei der Elektronen zwischen verschiedenen Substanzen übertragen werden. Oxidation bezieht sich auf den Verlust von Elektronen, während Reduktion den Gewinn von Elektronen beschreibt. In einer Redoxreaktion finden gleichzeitig Oxidation und Reduktion statt. Diese Art von Reaktionen sind für viele grundlegende Prozesse in der Chemie und Biologie verantwortlich, einschließlich Energiegewinnung und Stoffumwandlungen.
Was ist das Redoxpotential?
Das Redoxpotential, auch als Redoxwert oder Redoxspannung (nach DIN 38404-6) bezeichnet, ist ein Maß für die Neigung einer Substanz, Elektronen zu verlieren oder zu gewinnen, und es wird in der Regel in Millivolt (mV) gemessen. Es beschreibt die Fähigkeit einer chemischen Verbindung oder eines Systems, Elektronen zu übertragen, was wiederum anzeigt, wie oxidierend oder reduzierend dieses System ist. Ein höheres Redoxpotential bedeutet, dass das System eher oxidierend ist, während ein niedrigeres Redoxpotential auf eine größere Neigung zur Reduktion hinweist. Ein hohes Redoxpotential entsteht beispielsweise bei Sterilisationsmaßnahmen wie bei der Chlorierung von Wasser. Das Wasser wird dadurch zwar keimfrei, erhält aber stark oxidative Eigenschaften. Sinkt das Redoxpotential, kann dies auf organische Ablagerungen und Mikrobieller Aktivität hindeuten. Die organischen Stoffe dienen als Nahrung für Mikroorganismen, die sie abbauen. Während dieses Abbauprozesses können diese Mikroorganismen Sauerstoff verbrauchen, was zu erhöhten Redoxreaktionen und somit zu einem Abfall des Redoxpotentials führt.Autor / Verfasser: Marie-Luise Enghardt – M.Sc-Microbiology